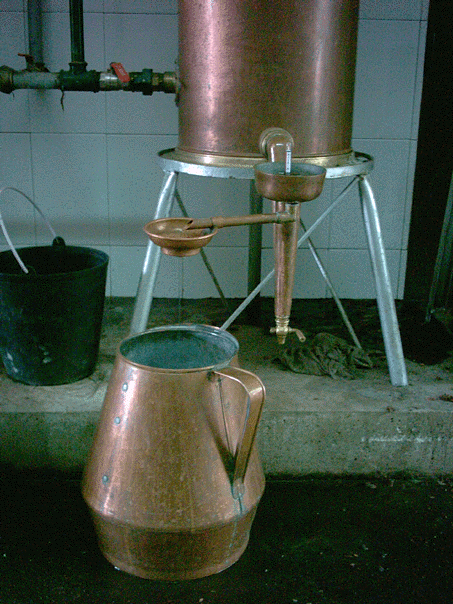|
|
|
| ADVERTENCIA: La elaboración de orujo es una actividad regulada y perseguida si se hace fuera de la ley (en España y algunos países), y muy peligrosa si se hace por aficionados. ¿QUE ES EL ORUJO? La normativa de la Unión Europea (Reglamento 1576/89) define el aguardiente de orujo, orujo o marc, como :
El orujo es un aguardiente obtenido por destilación de orujos de uva, es decir las partes sólidas de la vendimia que no tienen aprovechamiento en la previa elaboración del vino, perteneciendo al mismo tipo de bebida que los marc franceses, las grappas italianas, las bagaçeiras portuguesas o los tsiroupos griegos.
|
TÉCNICA DE ELABORACIÓN
Con la destilación de orujos no se pretende una simple extracción de alcohol, sino mas bien una extracción fina y selectiva de los componentes aromáticos contenidos en los orujos, mediante la concentración del alcohol casi 20 veces, y con el adecuado manejo de cabezas y colas, para obtener una bebida placentera para los sentidos, respetuosa con una tradición y una cultura, y que defina en sus características organolépticas la personalidad diferenciada de la materia prima de la que procede.
La técnica y el arte de la destilación consisten en regular el aporte externo de energía (calor), para conseguir un ritmo de destilación lento y constante, que permita la aparición de los componentes aromáticos deseados en los momentos adecuados.
El proceso de destilación se desarrolla en dos fases : la primera es la vaporización de los elementos volátiles de los orujos ; la segunda es la condensación de los vapores producidos.
En esta fase de condensación pueden distinguirse tres fracciones, que aparecen en el destilado en este orden : cabezas (con graduación alcohólica superior al 70% vol.), corazones (entre el 70% y el 45% vol.) y colas (menor de 45% vol.). Esta fragmentación es arbitraria.
Los trabajos realizados en la E.V.E.G.A. han permitido demostrar, entre otras cosas, que los ésteres, componentes que en general son favorables desde el punto de vista organoléptico, aparecen mayoritariamente en cabezas y corazones, mientras que compuestos indeseables como el metílico, la acetoína, el furfurol y ciertos ácidos orgánicos, aparecen fundamentalmente en las colas.
| Es muy importante, la correcta separación de las distintas fracciones del destilado, lo que requiere un permanente control sobre la graduación alcohólica de salida del destilado, aprovechando cabezas y corazones y rechazando las colas. La destilación de los orujos puede realizarse con aparatos de muy distintas características, aunque el reglamento de la Denominación Específica Orujo de Galicia admite solamente tres tipos ; de fuego directo : alquitara y alambique, y otro por arrastre de vapor. Aunque se diserte mucho sobre la superioridad de un método sobre otro en lo que se refiere a calidad del aguardiente de orujo obtenido, no hay elementos objetivos que permitan sustentar tal afirmación, no existiendo apreciaciones organolépticas diferenciales entre ellos, aunque parece que en determinadas circunstancias el alambique puede suministrar cantidades mayores de ésteres. |
Son por tanto criterios económicos los que han de primar en la elección del sistema. (alambique o alquitara)
La destilación
La experiencia secular ha establecido los patrones a los que obedece la técnica de la destilación artesanal.
Se inicia cargando la pota o caldera con 10-20 % de agua, previa colocación de sarmientos de vid o paja, o la base metálica de cobre perforada, para evitar el contacto directo de los orujos con el fondo de la pota o caldera, encendiendo el fuego. Mientras se calienta el agua se extraen los orujos de los recipientes de conservación. Se esparcen con un rastrillo, separando una porción más rica en raspón, que será la primera en introducirse en la pota o caldera, para conseguir una mejor circulación de los vapores en la masa del orujo, llenándola a continuación.
Cuando la salida e vapores es uniforme, se coloca el capacete (con el cuello de cisne o trompa de elefante en el caso del alambique), sellando las uniones con agua o masa de harina. A continuación se procede al llenado del depósito de refrigeración.
Es importante mantener el agua de refrigeración a temperaturas próximas a los 18-20 ºC. Temperaturas bajas provocan condensaciones rápidas que dan lugar a destilados duros ; mientras que, temperaturas altas provocan condensaciones lentas que dan lugar a la pérdida de componentes volátiles favorables.
Una vez iniciada la salida del destilado, se ha de procurar mantener un ritmo lento y uniforme, regulando adecuadamente el aporte de calor.
Los destiladores tradicionales (poteiros) recurrían a procedimientos artesanales para determinar el destilado aprovechable ; agitaban una muestra en un vaso para observar la persistencia de las burbujas y los frotaban entre las palmas de las manos valorando el olor. Aún admitiendo que la experiencia y destreza de los poteiros les permite alcanzar un notable grado de exactitud, nos parece más correcto, medir con alcohómetro las graduaciones de salida, para separar correctamente, cabezas, corazones y colas.
Se deben aprovechar las cabezas y corazones, rechazando las colas (graduaciones inferiores a 50 grados alcohólicos), aunque hay autores que recomiendan rechazar la primera fracción de las cabezas por considerar que van acompañadas de sustancias indeseables (sustancias sebáceas y sabor a cobre).
En todo caso, ésta es una decisión que ha de tomar el destilador en función de la calidad y estado de conservación de los orujos, así como de las características organolépticas percibidas en el destilado.
Luego procedemos a la limpieza y nueva carga del primer calderín.
Es importante que la presión del vapor se mantenga constante para que la salida del destilado sea regular
La preocupación principal en la destilación casera es la obtención no deseada del alcohol metílico, una sustancia toxica causante de muerte o con suerte, de ceguera permanente. Para evitar esto ha que separar siempre el buyo del sarmiento ya que es éste que generan el temido alcohol. En efecto el metanol se extrae fácilmente de la madera seca.
Algunas complementaciones sobre el orujo
Las destacadas bondades y características de una buen destilado de los orujos de uva dependen de muchos factores. De la misma variedad y calidad de uva, la modalidad familiar empleada en la extracción del mosto, la fermentación del mismo, el tiempo de conservación de los orujos hasta que se utilizan en el alambique y la composición de mismo. El porcentaje promedio por una uva de buena calidad lo podemos considerar compuesto de un 28% de raspones, 40% de hollejos, 30% de pepitas, 2% de otros elementos. El factor calidad de la materia prima y la buena conservación de los orujos para evitar la proliferación de microorganismos que pueden arruinar un destilado. El orujo se ha de conservar un tiempo para que los azúcares que contienen se trasformen en alcohol, También el excesivo prensado de las uvas influye sobre el rendimiento y la calidad de la destilación. La ruptura de las pepitas, ricas en aceite, pueden trasmitir aroma y gusto a rancio. Los raspones todavía verdes dan un gusto áspero, además, de producir alcohol metílico; en este caso la destilación de hacer enseguida luego de separar el vino. Luego de esta operación, en tos los casos, el periodo de espera debe considerarse de un mínimo de 15 días a un máximo de 3 meses. Periodos mayores aumentan el futuro destilado de metílico.
La composición de un litro de destilado de orujo, evidentemente no es todo alcohol. La destilación puede comenzar con un 70% de alcohol y un 30% de agua, pero puede terminar con un 30% de agua y 70% de alcohol. Así que podemos considerar un 38% como un porcentaje alcohólico satisfactorio. Si separamos el agua del alcohol, este se compone de un 99% de alcohol etílico, el 1% restante es alcohol etílico y otras sustancias. Según la ley, el limite máximo de metílico es 1.000g/Hl .
Por último podríamos hacer algunas distinciones entre orujos considerando:
Jóvenes aquellos que han sido puesto en recipiente que no aportan enriquecimiento alguno después de la destilación, es el caso de envasarlo en botella. Tienen un color blanco cristalino.
Añejados aquellos que han sido puesto en toneles de roble o de otra manera , donde adquieren caracteristicas distintas del momento de la destilación. Tienen un color blanco amarillento
Aromaticos, cuando por si mismos adquieren un aroma derivado de las variedades de uva, como moscatel, malvasía, etc.
Aromatizados, cuando interviene la maceración de hierbas medicinales y el orujo adquiere el color de los pigmentos contenidos en ellas. Por ejemplo un orujo aromatizado con mirto tiene un color rojo violáceo.
Para mayores explicaciones es mi opinión la consulta de libros sobre enología y destilados de alcoholes. Y la última opinión: lleve una muestra de su destilado a un laboratorio oficial para determinar si el porcentaje de alcohol metílico está dentro de la ley.
© Copyright 2002-2010. NURIA RAMÍREZ DE LA TORRE. Todos los derechos reservados.
fuente www.alambiques.com